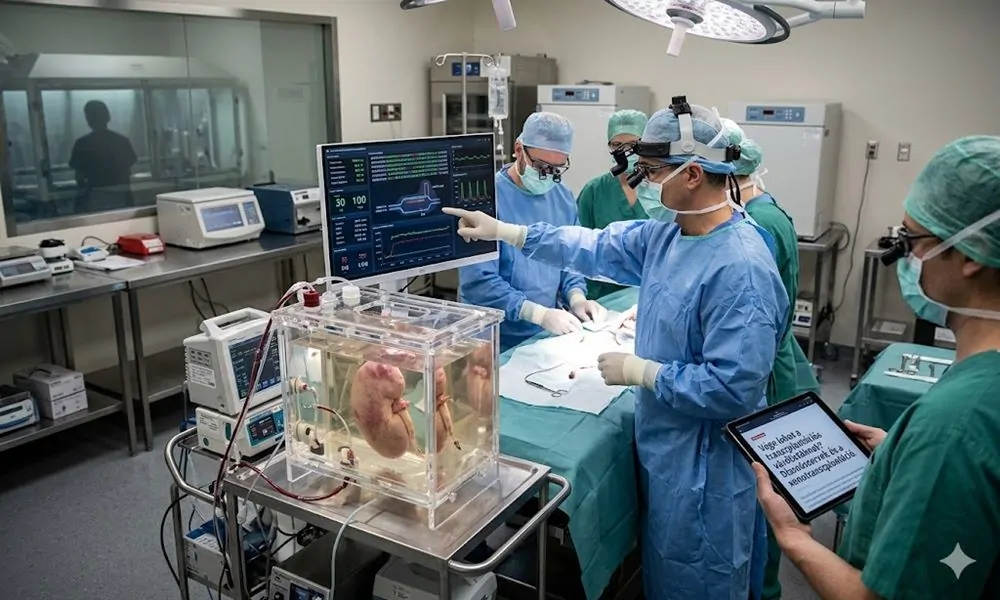
Van az orvoslásnak egy mondata, amelyet ritkán mondanak ki teljesen nyersen, mégis ott lüktet minden szervátültetés mögött: ahhoz, hogy valaki új szívet, májat vagy vesét kapjon, általában előbb meg kell halnia valaki másnak. A modern transzplantáció csodája egyszerre életmentés és hiánygazdálkodás. Az egyik ember túlélésének sokáig az volt a feltétele, hogy legyen mit átvenni egy másik testből.
Ez az a logika, amelyet a xenotranszplantáció – vagyis az állatból emberbe történő szervátültetés – most először látható közelségbe hoz ahhoz, hogy megtörjön. És bármennyire science fictionnek hangzik, a kérdés már nem az, hogy ez valaha megtörténhet-e, hanem az, hogy milyen gyorsan, milyen biztonsággal és milyen áron válhat valódi orvosi rutinná.
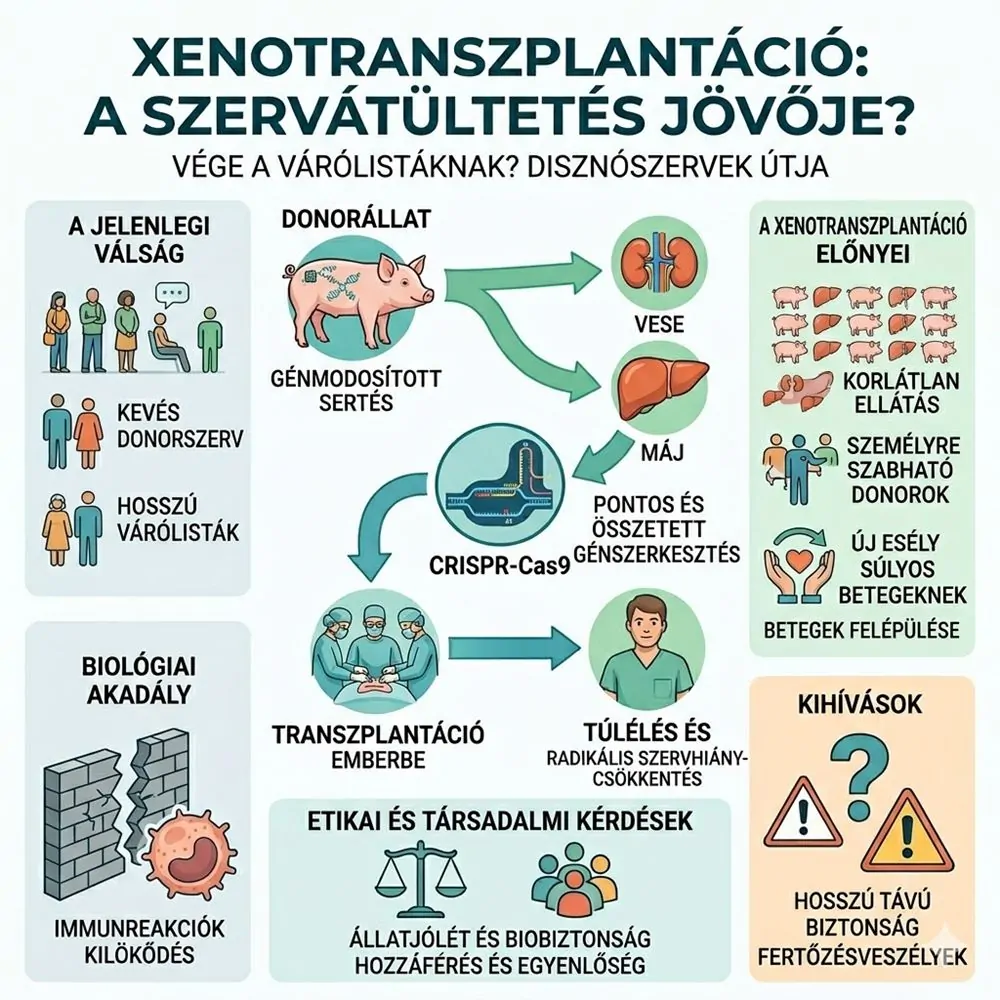
A várólisták problémája nem adminisztratív, hanem biológiai és kegyetlen
A szervátültetés ma már nem kísérleti kuriózum, hanem a modern gyógyítás egyik legnagyobb sikertörténete. Csakhogy a sikernek ára lett: minél jobb eredményeket érnek el az orvosok, annál több ember válik alkalmassá vagy jogosulttá a transzplantációra. A kereslet nő, a kínálat nem tud lépést tartani.
Az Egyesült Államokban jelenleg több mint százezer ember vár valamilyen szervre, és a legtöbben vesére. Eközben sokkal többen vannak azok, akik papíron profitálhatnának egy átültetésből, de soha nem jutnak el a listára, vagy azért, mert túl betegek lesznek, mire sorra kerülnének, vagy azért, mert a rendszer eleve nem számol reálisan az esélyeikkel.
A transzplantációs hiány tehát nem pusztán logisztikai probléma. Hanem egy olyan orvosi valóság, amelyben a döntések gyakran nem arról szólnak, ki gyógyítható meg, hanem arról, kinek jut egyáltalán esély.
Mi az a xenotranszplantáció, és miért pont most lett hirtelen komoly ügy?
A xenotranszplantáció lényege, hogy emberbe nem emberi eredetű sejtet, szövetet vagy szervet ültetnek át. Ezt az elképzelést sokáig a biomedicina egyik legmerészebb, egyben legkényesebb álmának tartották, mert az immunrendszer normál esetben villámgyorsan felismeri és elutasítja a más fajból származó szervet.
A helyzetet az változtatta meg, hogy a génszerkesztés az elmúlt években olyan pontosságúvá vált, amilyet néhány évtizede még csak jóslatként lehetett volna leírni. A kutatók ma már képesek több ponton is módosítani a donorállatok genomját: kiiktatni olyan molekulákat, amelyek azonnali immunreakciót váltanának ki, és hozzáadni emberi géneket, amelyek kompatibilisebbé tehetik az adott szervet az emberi szervezettel.
Ennek eredménye az, hogy a disznóból származó, erősen génmódosított vesék már nem pusztán laboratóriumi ígéretként szerepelnek a tudományos közbeszédben. Ma már vannak emberek, akik ilyen szervvel élnek, és közben klinikai vizsgálatok is futnak. Ez a terület 2026-ra látványosan átlépett az elméleti lehetőségből a korai klinikai valóságba.
Miért éppen a disznó lett a legígéretesebb donor?
A laikus első reakció gyakran az, hogy ha már állatból emberbe ültetünk át szervet, miért nem egy evolúciósan közelebbi főemlősből? A válasz egyszerre biológiai, technológiai és etikai.
A főemlősök szaporodása lassú, kevés utódot hoznak világra, és méretük sem mindig ideális. Emellett az emberszabásúak használata súlyos etikai ellenállásba ütközik, és fertőzésbiztonsági kérdéseket is felvet. A disznó ezzel szemben gyorsan szaporodik, egy alomban több malac születik, a szervei méretben jól közelítik az emberi szerveket, és az élelmiszeripari hasznosítása miatt társadalmi megítélése is más kategóriába esik.
Ez nem jelenti azt, hogy a disznó „tökéletes donor” lenne. Inkább azt, hogy a jelenlegi tudásunk szerint ez az az állat, amelynél a technológiai megvalósíthatóság, a méretarány, a tenyésztés és a génszerkeszthetőség együtt a legéletszerűbb utat kínálja.
A legnagyobb akadály sokáig az volt, hogy az emberi immunrendszer gyakorlatilag azonnal támadott
A korai xenotranszplantációs kísérletek egyik fő oka a gyors kudarcra az úgynevezett hiperakut kilökődés volt. A disznószervek sejtjeinek felszínén olyan cukormolekulák találhatók, amelyeket az emberi immunrendszer idegenként érzékel, és szinte azonnal támadásba lendül ellenük.
A kutatás egyik nagy fordulópontja az volt, amikor sikerült ezeket a célpontokat génszerkesztéssel kiiktatni, majd további olyan módosításokat beépíteni, amelyek mérséklik a gyulladást, a véralvadási zavarokat és az immunreakciók egy részét. A CRISPR-alapú génszerkesztés ezt a munkát nemcsak gyorsabbá, hanem jóval összetettebbé is tette: ma már nem egy-két, hanem akár tucatnyi genetikai módosítással dolgoznak a fejlesztések során.
Fontos kijózanítás: ez még nem rutin, és nem is kockázatmentes forradalom
A xenotranszplantáció körül könnyű lenne győzelmi indulót fújni, de ez még korai lenne. A legnagyobb kérdések továbbra sem tűntek el: mennyi ideig működik majd tartósan egy ilyen szerv, mekkora immunelnyomás szükséges hozzá, és milyen fertőzésbiztonsági kockázatok maradnak fenn hosszú távon.
Külön figyelmet kapnak az úgynevezett porcine endogenous retrovirusok, vagyis azok a vírusmaradványok, amelyek a sertések genomjába beépülve vannak jelen. Ezek klinikai jelentősége ma sem teljesen lezárt kérdés, ezért a biztonsági monitorozás a terület egyik legszigorúbban kezelt pontja. A kutatás tehát nemcsak arról szól, hogy működik-e a szerv, hanem arról is, hogy közben nem nyitunk-e ki egy új biológiai kockázati ajtót.
Ami most történik, az mégis történelmi léptékű
A legfontosabb fejlemény az, hogy a xenotranszplantáció már nem kizárólag kísérleti modellekben létezik. 2024-ben és 2025-ben több, nagy visszhangot kiváltó beavatkozás történt élő emberekben génszerkesztett disznóvesével, és 2025-ben hivatalosan is elindultak FDA-engedélyezett klinikai vizsgálatok ezen a területen. Ez nem jelenti azt, hogy a probléma megoldódott, de azt igen, hogy a kérdés mostantól nem elméleti, hanem klinikai.
A máj területén közben egy másik irány látszik erősödni: nem feltétlenül végleges átültetésként, hanem ideiglenes „biológiai híd” megoldásként, amely akut májelégtelenségben segíthet túlélni addig, amíg emberi donor nem érkezik. Ez különösen fontos lehet ott, ahol az időablak brutálisan rövid. 2026-ban már olyan eredmények is megjelentek, amelyek alapján génmódosított sertésmáj emberi keringéshez kapcsolva képes lehet átmeneti támogatást nyújtani.
A nagy kérdés nem az, hogy helyettesítheti-e az emberi donorokat, hanem hogy milyen sorrendben és kiknél
A közhiedelemmel ellentétben a xenotranszplantáció első sikere valószínűleg nem az lesz, hogy holnaptól mindenki disznóvesét kap a várólista helyett. Sokkal valószínűbb, hogy először azoknál a betegeknél válik valódi opcióvá, akiknek nagyon kicsi az esélyük megfelelő emberi donorhoz jutni, vagy akiknél ideiglenes, áthidaló megoldásra van szükség.
Magyarul: ez a technológia először nem feltétlenül kiváltani fogja a jelenlegi rendszert, hanem kitágítani. Először a legreménytelenebb helyzetekben adhat időt, második esélyt, túlélést. Aztán, ha a hosszú távú eredmények valóban javulnak, fokozatosan egyre több betegcsoport számára válhat reális alternatívává.
És itt jön a legkényelmetlenebb, de legfontosabb etikai kérdés
Ha valóban korlátlanul előállítható, személyre szabható vagy legalább nagy volumenben tenyészthető donorállatokból származó szervekhez jutunk, az nemcsak orvosi áttörés lesz, hanem társadalmi földrengés is. Újra kell gondolni, kit tekintünk jogosultnak transzplantációra, hogyan változik a donorhiány köré épült rendszer, és hol húzódik az állatjólét, a biobiztonság és az emberi életmentés közti határ.
Mert miközben a jelenlegi rendszer kegyetlenül szűkös, legalább részben a hiány szabályozza. Egy bőségesebb jövő egészen más típusú döntéseket hoz majd: nem azt kell mérlegelni, ki kapjon egyáltalán esélyt, hanem azt, milyen áron, milyen feltételekkel és milyen hosszú távú következményekkel tágítjuk ki az emberi test határait.
Science fiction? Igen. Csakhogy már a műtőajtón innen
A xenotranszplantáció ma még nem hétköznapi orvosi gyakorlat. De már nem is puszta jövőkép. Az, hogy emberek génmódosított disznóvesével élnek, hogy szabályozott klinikai vizsgálatok indultak, és hogy a májtámogatásban is kézzelfogható eredmények jelennek meg, azt jelzi: ez a forradalom nem a távoli jövő zenéje, hanem egy most formálódó korszak első, zajos, bizonytalan, de nagyon is valós hangpróbája.
Lehet, hogy még évek kellenek hozzá, mire egy betegnek azt mondják: nem kell várni egy ismeretlen donor tragédiájára, mert a szerv már készül. De az a világ, amelyben ez elképzelhető, már nem a fantázia terepe. Már az orvostudomány tárgyalóasztalán van.
Amit ebből most érdemes megjegyezni
A xenotranszplantáció lényege nem az, hogy „disznószervet ültetnek emberbe”, hanem az, hogy a modern génszerkesztésnek köszönhetően először látszik technológiailag megvalósíthatónak a donorhiány radikális csökkentése. A terület jelenleg főleg a vesével halad előre, mert ott a klinikai szükséglet óriási, a túlélést támogató alternatíva – a dialízis – létezik, és a kockázatok bizonyos fokig jobban kezelhetők. A következő nagy kérdés az lesz, hogy a mostani korai sikerekből tartós, hosszú távú működés lesz-e, és hogy a fertőzésbiztonsági, immunológiai és etikai akadályok milyen gyorsan oldhatók fel.
Források
Tatsuo Kawai, Leonardo V. Riella, Nahel Elias és mtsai: első élő emberben végzett, génszerkesztett sertésvese-átültetés klinikai közlései és kapcsolódó transzplantációs beszámolók.
Yue Shen, Lin Wang, Jianmin Wang és mtsai: First-in-human temporary bridge support with a genetically modified porcine liver in a patient with acute-on-chronic liver failure.
A porcine endogenous retrovirusokkal és a xenotranszplantáció fertőzésbiztonsági kérdéseivel foglalkozó elsődleges szakirodalmi közlések a 2025–2026-os időszakból.